■目次(押すとジャンプします)
酸塩基平衡を維持するメカニズム3つ
秒〜分単位
重炭酸イオン緩衝系、細胞内蛋白緩衝系などの化学的な緩衝作用により、急激なpHの上昇が抑制
分〜時間単位
揮発性の炭酸ガスは肺から呼気として排泄
時間〜日単位
リン酸、硫酸、乳酸などの不揮発酸は、腎臓から近位尿細管における重炭酸イオンの再吸収、ないしは、皮質集合管での重炭酸の産生により排泄。
酸塩基平衡の解析には、様々あるが、ここでは日常臨床よく用いられるBoston法を紹介します。
血液ガスの読み方
- アシデミアかアルカレミアか
- 代謝性か呼吸性か
- 代償性変化が予測の範囲内か
- アニオンギャップ(AG)の計算
- AGが正常としたときの推測重炭酸イオン(HCO3-)の計算
アシデミアかアルカレミアか
pH が 7.40 より低い(アシデミア)または高い(アルカレミア)かをみる。またpHが正常であっても、アシドーシスとアルカローシスの両方が同時に存在し同程度に生じていることがある。
代謝性か呼吸性か
アシデミアまたは、アルカレミアに向かわせている一次性の異常は代謝性か呼吸性かをみる。
HCO3をアルカリ物質、PCO2を酸性物質と考えるとわかりやすい。
アシデミアがある場合
HCO3が低い(代謝性アシドーシス)か、PCO2、が高い呼吸性アシドーシス)か、そのどちらか、あるいは両方であることが考えられる。
アルカシミアがある場合
HCO3が高い(代謝性アルカローシス)か,PCO2が低い(呼吸性アルカローシス)か, あるいは両方であることが考えられる。
代償性変化が予測の範囲内か
代償性変化が予測の範囲内か確認し、代償不足・過剰を起こしている酸塩基平衡異常が合併していないか検証する。生体は一次性の異常に対し代償性機構を働かせて pH を正常方向に戻そうとする、予測される代償性変化の範囲を表に示す。
| 一次性病態 | 一次性変化 | 初期のpHの変化 | 代償性変化 | 予測範囲 |
| 代謝性アシドーシス | ↓HCO3 | ↓↓pH | ↓PCO2 | ⊿PCO2=(1.0~1.3)×⊿HCO3 |
| 代謝性アルカローシス | ↑HCO3 | ↑↑pH | ↑PCO2 | ⊿PCO2=(0.5~1.0)×⊿HCO3 |
| 呼吸性アシドーシス | ↑PCO2 | ↓↓pH | ↑HCO3 | 急性⊿HCO3=0.1×⊿PCO2 慢性=0.35×⊿PCO2 |
| 呼吸性アルカローシス | ↓PCO2 | ↑↑pH | ↓HCO3 | 急性⊿HCO3=0.2×⊿PCO2 慢性=0.5×⊿PCO2 |
実際の代償性変化と予測される範囲を比較し、代償性変化の不足・過剰を検証する。しかし,日常診療の現場でこの関係式
を計算するのはやや煩雑であるため、臨床上とくに問題となる代謝性異常について、簡便で日常診療で役に立つ裏技がある。
| 代償性変化の予測範囲 |
| 代謝性アシドーシス:⊿PCO2=(1.0~1.3)×⊿HCO3 代謝性アルカローシス:⊿PCO2=(0.5~1.0)×⊿HCO3 |
| ⊿PCO2=(おおむねで1.0を採用)×⊿HCO3 40-PCO2=1.0×(25-⊿HCO3) ⊿HCO3基準値としておおむね25を採用 =25-HCO3 予測PCO2=HCO3+15 |
実測PCO2がこの予測値(HCO3+15)より小さければ、呼吸性代償の過剰があり、呼吸性アルカローシスを合併している
アニオンギャップの計算
アニオンギャップ(anion gap:AG)が増大している代謝性アシドーシスの有無を確認する。AG=Na-(Cl + HCO3) を計算する。AGが高ければ何らかの異常な不揮発性酸の蓄積を示していることとなり、AG 増大代謝性アシドーシスの存在を意味している。
AGが正常としたときの推測重炭酸イオン(HCO3-)の計算
AGが増大している場合、AG が正常であったとしたときの推測HCO3を計算する。AG が増大しているとき、不揮発性酸が蓄積し余分なHを中和するために HCO3が消費されていると考え、AGが増大していないと仮定した場合の HCO3を推測することで、さらに隠れた代謝性異常の存在を検証する。
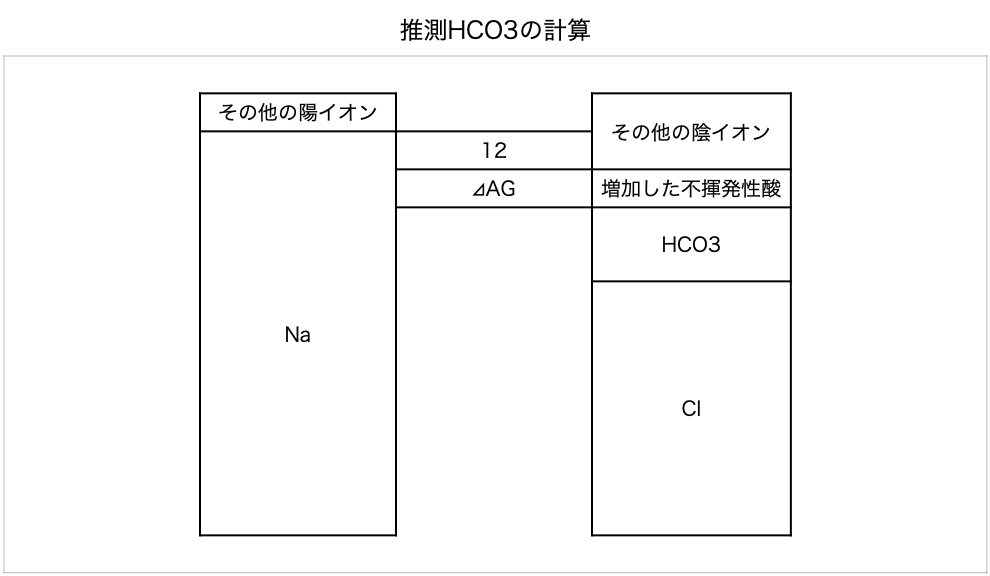
推測 HCO3= 実測 HCO3+ ⊿AG-HCO3+(Na-C1-HCO3-12) = (Na-Cl) -12
酸塩基平衡異常の原因・治療(代謝性異常)
これらの解析によって、代謝性アシドーシス・アルカローシス、呼吸性アシドーシス・アルカローシスの4種の酸塩基平衡異常が導き出されるが、なかでも代謝性異常、とくに代謝性アシドーシスは、重症疾患に伴ってよくみられ臨床で難渋することが多い。
以下、代謝性異常を中心に述べる。
代謝性アシドーシス・アルカローシスの主な原因を表に示す。
| AG増大の代謝性アシドーシス | AG正常の代謝性アシドーシス | 代謝性アルカローシス |
| 内因性物質によるもの 腎不全 ケトアシドーシス(糖尿病、アルコール、飢餓、乳酸アシドーシス、敗血症、痙攣) 外因性物質によるもの メタノール、サリチル酸エチレングリコール、asprin、NSAIDs など | 腸管からのHCO3-の喪失 下痢 尿管S状結腸吻合、人工肛門 腎でのHCO3-喪失 尿細管性アシドーシス2型acetazolamide内服 低アルドステロン症 腎でのH+排泄障害 尿細管性アシドーシス1型 腎不全 Clの負荷 大量輸液負荷 アミノ酸製剤負荷 sevelamer hydrochloride | H+の消化管からの喪失 嘔吐、胃液吸引 H+の腎からの喪失 アルドステロン症 偽性アルドステロン症 利尿薬(ループ、サイアザイド) 高Ca血症 H+の細胞内シフト 低K血症 HCO3-の増加 重炭酸Na投与 輸血(クエン酸を含む) |
代謝性酸塩基平衡異常に対する補正
代謝性アシドーシス
代謝性アシドーシスの治療は、原因となっている基礎疾患自体の治療が重要かつ根本的であり、多くの場合は十分である。たとえば、A型乳酸アシドーシスの原因は組織低酸素であり、組織の循環改善と酸素化の確保が必要で、細胞外液補充、昇圧薬投与、輸血、酸素投与、人工呼吸管理などを病態に応じて行う。糖尿病性ケトアシドーシスでは、生理食塩水による脱水の改善、インスリン投与、電解質補正(低 K,低P)が治療となる。
高度の代謝性アシドーシス
代謝に与える影響
高度の代謝性アシドーシス(pH 7.1 未満)では、酵素や受容体などの蛋白にHが結合し,その物理化学的性質が変性する。たとえば、解糖系のホスホフルクトキナーゼは抑制され、ATP産生は著しく阻害される。
循環器系への影響
心血管系への影響はとくに重要で,血管と心筋のカテコラミンに対する反応性は減弱し、心筋では H+が電位依存性 Caチャネルによる細胞内Ca取込みを阻害する。動脈拡張・心収縮力減弱により血圧低下し、心室性不整脈も誘発されやすく、循環動態の破綻を引き起こす。
ショックなどによる乳酸アシドーシスは問題となる
高度なアシドーシスであっても、可逆的な基礎疾患による一過性のものであれば重篤な状態とならないこともあり、その持続性が重要となる。とくに問題となるのはショックなどによる高度の組織低酸素による乳酸アシドーシスで、急速かつ持続的に酸(乳酸)が産生され、産生量が肝での有機酸代謝と腎からの酸排泄のスピードを上回り、急激に状態が悪化する場合がある。
緊急的治療の目的での重炭酸 Na の経静脈投与の是非については、臨床的な無作為試験データもほとんどなく一定した見解が得られていない。アシドーシスの程度が高度かつ進行性
で予後を左右するような緊急性の高い場合には、アシドーシス自体への治療として重炭酸 Na投与が考慮される。まずは pH7.2 が治療の目標となる。換気による呼吸性代償は非常に重要であり、代償反応が正常であれば、pH7.2 は HCO3-濃度にして8~10 mEq/Lに相当するため、換気が充分に確保された状態では、HCO濃度として10 mEq/L を保つとよいということとなる。
重炭酸Na投与による補正
重炭酸 Na投与による補正には後述のように肺胞換気が適正に行われていることが必須であり、必要に応じて人工呼吸管理も行い、換気を十分に確保する(呼吸性アルカローシスの誘導)。分布容積を理想体重の50%,目標 HCO3濃度10 mEq/Lとして、重炭酸 Naの必要補充量を推算すると、(10 – 実測 HCO3濃度)×理想体重×0.5(mEq)となる。経静脈投与する際は、1回に1~2 mEq/kg 体重を超えない量を30分~2時間程度かけて投与する256)。 血液ガスや電解質を1~4時間ごとにモニターする。異常な酸産生が持続し産生速度が速い場合は推算量より多くするのが必要となる一方で、基礎疾患の治療で血圧が改善し肝での乳酸代謝が回復すると急速な過剰補正を引き起こす可能性があり注意が必要である。
重炭酸 Na投与を行う場合に注意すべきこと
体内に HCO3を投与するとCO2が産生されるが、その産生量は代謝性アシドーシス下で増大し、細胞膜の CO2透過性がHCO3よりも高いために、換気の低下、あるいは組織での灌流障害がある場合には、産生された CO2は HCO3よりも速やかに細胞内に拡散し,細胞内 pH が奇異性に減少する可能性がある(いわゆる「奇異性細胞内アシドーシス」)、そして乳酸アシ
ドーシスはさらに増悪する、また、イオン化Caが減少し低Ca血症をきたす。これらのリスクは重炭酸 Naの投与が一般的に推奨されていない理由となっている。
このように,重炭酸 Na投与を行う場合には、細胞外液量過剰、低K血症、低Ca血症、奇異性細胞内アシドーシスなど有害な作用を生じる可能性を常に念頭に置いて診療する必要がある。
なお、透析療法でも,重炭酸 Na 中心静脈投与と同様に HCO3を投与することになるが、乳酸除去効果があり、低Ca血症を予防でき、体液量を調節できることから、これらの有害事象
を減らすことを期待して行われていることが多く、透析の是非については中心静脈投与に比して議論が少ない。
また、重炭酸 Naに代わる THAM (trometh-amine). carbicab (炭酸 Na/重炭酸 Na 混合物)といった CO2産生の少ない緩衝液も試みられているが、臨床使用例は少なく今後の検討が必要である
代議性アルカローシス
代謝性アルカローシスが維持されるメカニズム
- 有効循環血漿量低下による近位尿細管でのHCO3-再吸収増加
- GFR(glomerular filuration rate)低下による HCO3 排泄低下
- クロール(chlorine : CI) 欠乏による皮質集合管での HCO3-分泌低下
- K欠乏による近位尿細管での HCO3-再吸収増加
- 皮質集合管でのH+排泄増加および H+の細胞内シフト
があげられる。代謝性アルカローシスにおいても基礎疾患自体の治療が重要かつ根本的であるが、加えてこれらの因子を是正することが治療の基本となる。
細胞外液補充時に注意すること
細胞外液が補充されると、HCO3-排泄が増加し,それに伴いKも喪失するため、K 補充が必要となる。生理食塩水に K 10~20 mEq/L以下の濃度で通常 20 mEq/時まで(最大40 mEq/時)の速度になるように KCIを調整した溶液を用い、血清Kと心電図をモニターしながら投与する。Mg欠乏にも留意する。
細胞外液量が減少していない Cl抵抗性代謝性アルカローシスでの補正
acetazolamide や抗アルドステロン薬(spironolactone, eplerenone) も適応であり電解質に注意しながら用いる。
高度の代謝性アルカローシス (pH>7.6) で、活動性の心血管障害を有する場合や、テタニー、痙攣、不整脈などの症状を呈している場合
アルカローシス自体への治療も考慮される。方法としては、必要に応じて人工呼吸器管理を用いて、十分な酸素化を確保したうえでの低換気による呼吸性アシドーシスの誘導、低重炭酸イオン濃度の透析液を用いた透析、透析ができない患者では塩酸あるいは塩化アンモニウムの投与があげられる。塩酸投与については、0.1~0.15 N (0.1~02N)の塩酸を蒸留水あるいは1/4生理食塩水に溶解して作成し、100~150mEq/8~24時間かけて(0.2 mEq/体重kg/時を超えないようにする)、酸抵抗性フィルターを用いて経中心静脈投与する。1~2時間ごとに血液ガスや電解質をモニターしながら治療する。カテーテルやチューブは耐食性を考慮して選択し12時間ごとに交換する。塩酸は血管内溶血や組織壊死など食な副作用をもたらすことがあり細心の注意が必要となる。